手性硅化合物在化学合成、制药工业和材料科学等领域具有广泛的应用。其中,具有硅立体中心(Si-stereogenic center)的化合物因其独特的结构和性质而备受关注。然而,通过不对称催化合成具有硅立体中心的化合物一直是一个挑战。这主要是因为C−Si键比C−C键更长,且含硅的不饱和键不稳定。尽管已有研究通过过渡金属催化的炔烃反应来合成手性硅化合物,但这些方法存在一定的局限性,例如反应选择性不足或底物范围有限。
1. 手性硅立体中心化合物的重要性
手性硅立体中心(Si-stereogenic center)化合物在多个领域具有重要的应用价值:
化学合成:手性硅化合物是许多有机合成中的关键中间体,能够用于构建复杂的分子结构。
制药工业:手性硅化合物可以作为药物合成中的重要前体,用于合成具有特定生物活性的分子。
材料科学:手性硅化合物在光学材料、半导体材料等领域也有重要应用,尤其是在需要手性诱导的材料中。
光学和电子学:手性硅化合物在圆偏振发光(CPL)材料和有机电子器件中具有潜在的应用价值,因为它们可以通过手性诱导实现特定的光学和电子性质。
2. 合成手性硅立体中心化合物的挑战
尽管手性硅化合物具有广泛的应用前景,但其合成一直面临诸多挑战:
C−Si键的特性:C−Si键比C−C键更长,且含硅的不饱和键(如Si=C键)相对不稳定。这使得在不对称催化中构建硅立体中心更加困难。
现有方法的局限性:
反应选择性不足:炔烃的不对称氢硅化反应通常只能生成三取代的硅立体中心化合物,难以合成四取代的硅立体中心化合物。
底物范围有限:某些方法(如硅杂环丁烷的开环反应)对末端炔烃不兼容,且在非对称内部炔烃的情况下难以控制区域选择性。
合成步骤繁琐:一些方法需要多步合成前体化合物,增加了合成的复杂性和成本。
炔烃的过渡金属催化反应:大多数已报道的合成手性硅立体中心的方法依赖于过渡金属催化的炔烃反应,例如炔烃的氢硅化反应或硅杂环丁烷的开环反应。然而,这些方法存在以下问题:
其他方法的限制:尽管近年来有一些突破,例如通过不对称质子硼化实现硅立体中心的去对称化,但这些方法的底物范围仍然有限,且需要复杂的前体化合物。
鉴于现有方法的局限性,研究团队提出了开发一种新的高效方法,以实现从简单烯烃合成手性硅立体中心化合物的目标:
简单烯烃的优势:简单烯烃是一类丰富且廉价的化学原料,广泛用于有机合成。如果能够从简单烯烃直接合成手性硅立体中心化合物,将极大地简化合成步骤,降低成本,并提高合成的原子经济性。
研究目标:开发一种高效的不对称催化体系,能够在温和条件下从简单烯烃合成具有高对映选择性的四取代硅立体中心乙烯基硅烷。该方法应具有广泛的底物适用性、良好的官能团耐受性,并能够实现从石油衍生的异构体混合物中高效合成单一区域和立体异构体产物。
4. 研究团队的前期工作和灵感来源
Ni催化的研究基础:研究团队受到Ni催化的硅杂环丁烷与末端烯烃的硅化反应的启发,该反应具有广泛的底物适用性和无需氢受体的优点。然而,Ni催化的反应在内部烯烃的立体化学控制方面存在挑战。
铑催化的研究进展:近年来,铑催化的C−Si键切断反应取得了显著进展。研究团队推测,铑催化的体系可能在控制立体化学方面具有独特的优势,因此尝试开发一种基于铑催化的不对称硅化反应。
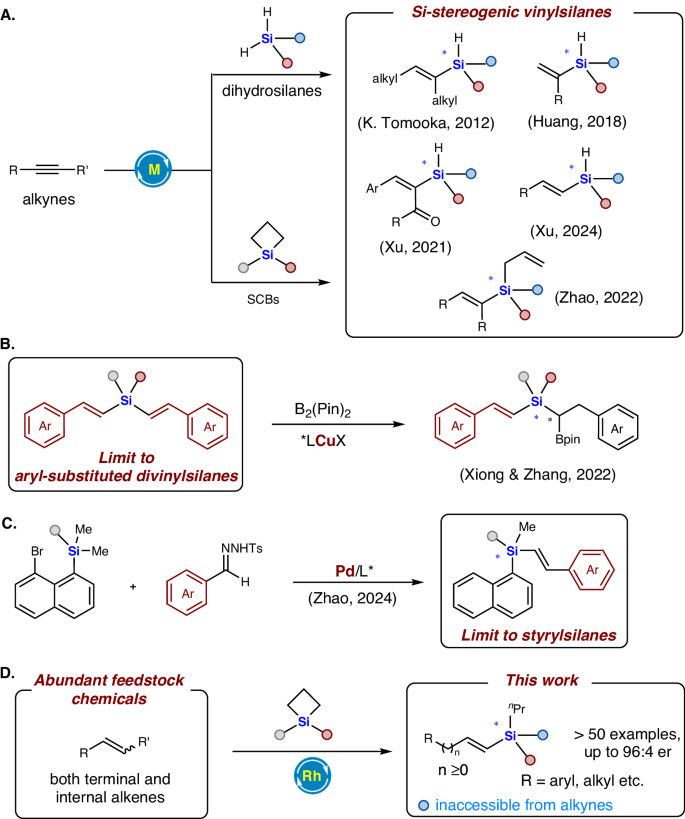
研究者们开发了一种铑(Rh)催化的体系,能够从简单的烯烃高效合成具有硅立体中心的手性乙烯基硅烷。这一方法的关键在于使用了特定的配体(如L25和L26),这些配体在反应中起到了关键作用,能够控制反应的对映选择性。反应条件经过优化,包括溶剂、铑前催化剂、碱、添加剂、反应温度和时间等。最终,研究者们实现了从简单烯烃到手性硅立体中心乙烯基硅烷的高效转化。
反应条件优化:通过筛选不同的配体、溶剂、催化剂前体等,研究者们找到了最佳的反应条件。例如,使用(Rp, R)-FOXAP配体时,反应产物的对映选择性(ee)和产率均较高。进一步优化后,使用L25配体在n-庚烷溶剂中,结合LiOBu作为添加剂,在100°C下反应48小时,得到了较高的产率和对映选择性。
底物范围探索:在优化条件下,研究者们测试了多种底物,包括不同取代的苯乙烯衍生物、杂芳基烯烃、以及内部烯烃等。结果显示,这些底物均能很好地参与反应,生成相应的产品,并且具有良好的产率和对映选择性。
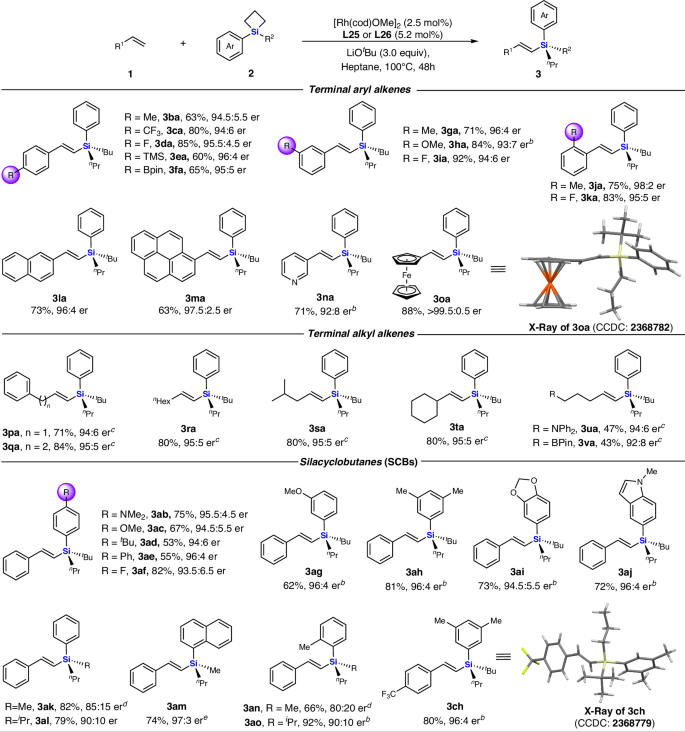
底物适用性
合成应用
1. 手性乙烯基硅烷3aa的合成应用
手性乙烯基硅烷3aa作为平台分子,可以进一步转化为多种手性硅化合物,具有广泛的合成应用前景。文章中展示了以下几种下游转化反应:
(1)溴化反应:3aa在溴化试剂的作用下进行溴化反应。生成了溴代产物6,产率为75%,对映选择性为93.5:6.5 er。溴化反应可以将乙烯基转化为溴代基团,为进一步的偶联反应提供了便利。
(2)环氧化反应:3aa在适当的氧化剂作用下进行环氧化反应。生成了环氧化产物7,产率为95%,对映选择性为94:6 er。环氧化反应可以将乙烯基转化为环氧基团,用于合成具有特定生物活性的化合物。
(3)几何异构化反应:3aa在光化学条件下进行几何异构化反应。生成了Z构型的产物8,产率为58%,对映选择性为95:5 er。几何异构化反应可以改变双键的构型,从而影响分子的性质和反应性。
(4)全面氢化反应:3aa在Yu的芳烃氢化条件下进行氢化反应。生成了全饱和的产物9,产率为97%,对映选择性为92:8 er。氢化反应可以将所有不饱和键(包括苯环)还原为饱和键,用于合成具有特定物理化学性质的化合物。
(5)氧化反应:3aa在适当的氧化条件下进行氧化反应。生成了酰基硅烷10,产率未提及,但对映选择性保持较高。氧化反应可以将乙烯基转化为酰基,用于合成具有特定官能团的化合物。
(6)硼氢化反应:3aa在不同的催化体系和硼试剂作用下进行硼氢化反应。生成了硼氢化产物11和12,产率和对映选择性未提及,但展示了位点选择性的调控。硼氢化反应可以将乙烯基转化为硼氢化基团,用于合成具有特定反应性的化合物。
(7)硅基转化反应:3aa的苯基硅基可以被直接转化为羟基。生成了手性硅醇13,产率未提及,但对映选择性保持较高。硅基转化反应可以将硅基从苯基转化为羟基,用于合成具有特定官能团的化合物。
(8)选择性还原反应:13的羟基可以被选择性还原为氢硅烷15,同时形成硅醚14。生成了手性氢硅烷15和硅醚14,产率未提及,但对映选择性保持较高。选择性还原反应可以将羟基转化为氢硅烷,用于合成具有特定反应性的化合物。
(9)C=C键的选择性氢化反应:3aa的C=C键可以被选择性氢化。生成了产物16,产率为93%,对映选择性为95:5 er。选择性氢化反应可以将C=C键还原为单键,用于合成具有特定物理化学性质的化合物。
2. 手性π-共轭双键体系的开发
文章中进一步展示了如何利用手性乙烯基硅烷3aa开发手性π-共轭双键体系。这些体系在功能材料和光学材料中具有重要应用价值。
(1)合成方法:使用二烯和三烯(如1,4-二乙烯基苯和1,3,5-三乙烯基苯)与硅杂环丁烷2a在优化的铑催化条件下进行反应。合成了四种手性π-共轭双键体系17、18、19和20,这些化合物均具有手性硅立体中心。这些手性π-共轭双键体系在光学材料和功能材料中具有潜在应用价值,尤其是在需要手性诱导的材料中。
(2)光物理性质:所有四种化合物均表现出荧光,具有不同的发射波长和强度。其中,化合物19具有最长的最大发射波长和最高的量子产率(Φf),在固态和溶液中分别为0.73和0.87。荧光性质表明这些化合物在光学材料中具有潜在应用价值,尤其是在需要特定发射波长和高量子产率的材料中。
(3)圆二色光谱(CD)和圆偏振发光(CPL):化合物17、19和20及其对映体在CHCl₃中表现出明显的Cotton效应,表明这些化合物具有手性光学性质。尽管这些化合物在溶液和固态中均未表现出CPL活性,但其CD光谱表明它们具有手性光学性质。这些手性π-共轭双键体系在圆偏振发光材料中具有潜在应用价值,尤其是在需要手性诱导的光学材料中。
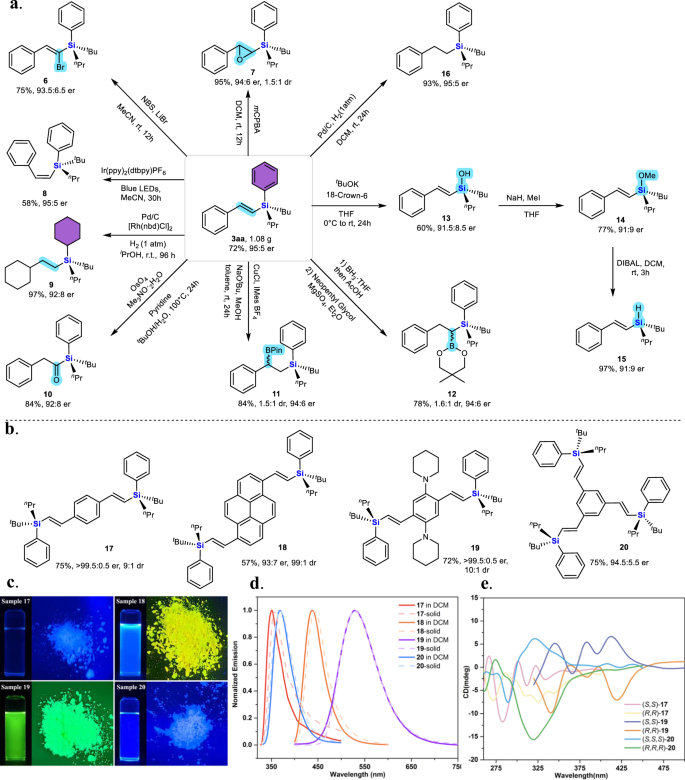
合成应用
机理验证
(1)催化剂的活性物种:研究者们通过合成一个预催化剂L26-Rh-H(图6a),并将其用于反应中。实验结果表明,使用L26-Rh-H作为催化剂时,反应能够顺利进行,生成目标产物3aa,产率达到86%,对映选择性为94:6 er(图6b)。这一结果证实了[Rh]-H物种在反应中的活性作用。实验结果表明,铑催化剂中的[Rh]-H物种是反应的活性催化剂。
(2)氘代实验:研究者们使用2,2'-二氘代苯乙烯(1a-D₂)作为底物,分别在Ni催化和Rh催化条件下进行反应。在Ni催化条件下,氘原子选择性地转移到丙基末端位置。在Rh催化条件下,氘原子不仅出现在丙基末端位置,还在苯乙烯的β位检测到氘原子(图6c)。氘代实验结果表明,Rh催化体系中的反应机制与Ni催化体系不同。Rh催化条件下,氘原子在多个位置的分布表明反应可能涉及多个步骤,包括C-H键的插入和迁移。
(3)非线性效应研究:研究者们通过改变手性配体L25的浓度,观察产物3aa的对映选择性变化。实验发现,产物3aa的对映选择性与配体L25的浓度呈线性关系(图6d)。这一结果表明,反应中只有一个手性配体参与每个对映选择性决定的过渡态,进一步支持了[Rh]-H物种作为活性催化剂的假设。
理论计算(DFT)
为了深入理解反应机制和对映选择性的来源,研究者们进行了密度泛函理论(DFT)计算。计算模型以苯乙烯1a与硅杂环丁烷2a的反应为模型反应,计算水平为MN15(SMD)/SDD&6-311+G(d,p)//B3LYP-D3(BJ)/SDD&6-31G(d)。
(1)反应路径和能量分析
反应路径:计算的反应路径从L26-Rh-H活性催化剂开始,涉及以下步骤(图6e):
Si-C键的氧化加成:通过过渡态(S)-TS1,形成五元环铑中间体(S)-IM1。
C-H键的还原消除:通过过渡态(S)-TS2,生成Rh-硅烷中间体(S)-IM2。
烯烃的配位和插入:烯烃1a配位到Rh中心,形成中间体(S)-IM3,随后C=C键插入Rh-Si键,形成中间体(S)-IM4。
β-H消除:通过过渡态(S)-TS4,释放产物3aa并再生活性催化剂。
能量分析:计算结果表明,Si-C键的氧化加成是反应的决速步骤,也是对映选择性决定步骤。计算得到的(S)-TS1和(R)-TS1之间的能量差为2.3 kcal/mol,对应于373.15 K时的对映选择性比率为96:4,与实验结果非常吻合(图6e)。
(2)对映选择性的来源:优化的过渡态几何结构(图6f)显示,在(S)-TS1中,铑与苯基之间存在Rh···Ph相互作用,而在(R)-TS1中,这种相互作用更为显著。然而,(R)-TS1中硅杂环丁烷(SCB)部分与配体之间的空间位阻更大,导致(R)-TS1的能量高于(S)-TS1。空间位阻是导致对映选择性的主要原因。在(S)-TS1中,SCB部分远离配体,而在(R)-TS1中,SCB部分靠近配体,导致更大的空间位阻。这种差异使得(R)-TS1的能量更高,从而导致反应倾向于生成(S)-构型的产物。
机理验证
反应机理
通过实验和理论计算,研究者们揭示了铑催化的不对称硅化反应的详细机制:
活性物种:[Rh]-H物种是反应的活性催化剂。
决速步骤:Si-C键的氧化加成是反应的决速步骤,也是对映选择性决定步骤。
对映选择性来源:空间位阻是导致对映选择性的主要原因,反应倾向于生成能量更低的过渡态对应的产物。
反应路径:反应通过一系列明确的中间体和过渡态进行,包括氧化加成、还原消除、烯烃插入和β-H消除。
